Induction et retard de détection
Homme de 27 ans avec syndrome de Brugada; implantation d'un défibrillateur sous-cutané A209 Emblem; programmation pour la procédure d'induction: Thérapies On, 1 zone (une zone de choc à 230 bpm), stimulation post-choc sur On; gain sur 1X, vecteur primaire.
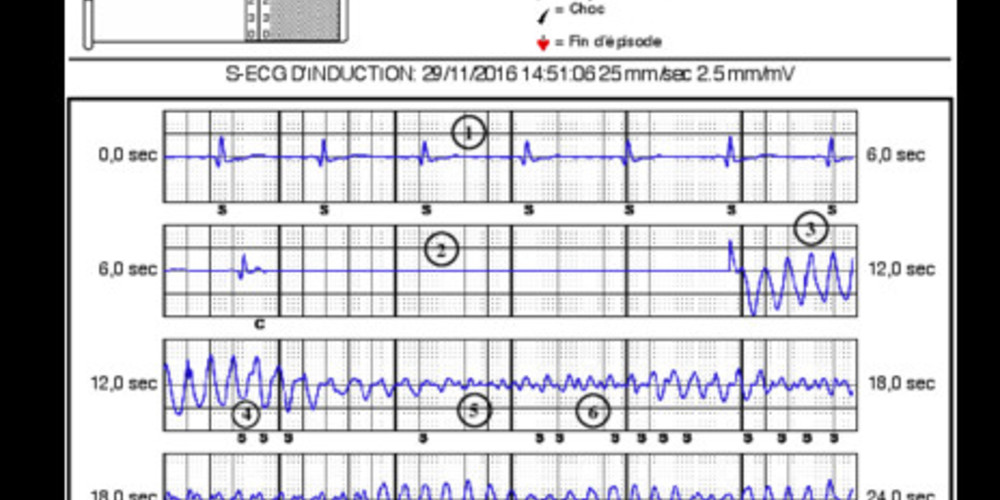
- rythme sinusal;
- burst 50 Hz délivré pendant 4 secondes environ;
- induction d'une FV (arythmie rapide, polymorphe, anarchique);
- premier cycle détecté classé S;
- plage de sous-détection devant l'atténuation de l'amplitude des signaux;
- détection intermittente de l'arythmie;
- premier cycle classé T, la moyenne des 4 intervalles précédents correspondant à la zone de tachycardie; le profil de sensibilité est modifié;
- détection correcte de l'arythmie avec cycles consécutifs classés T (en dépit de la non détection de quelques complexes);
- le compteur 18/24 est rempli ainsi que la persistance; début de la charge des condensateurs;
- poursuite de l'arythmie pendant la charge avec détection correcte;
- confirmation de l'arythmie en fin de charge;
- choc délivré (65 Joules) après 19 secondes d'arythmie;
- blanking post-choc;
- choc efficace et retour du rythme sinusal correctement détecté par le dispositif.
Femme de 41 ans avec myocardiopathie hypertrophique; implantation d'un défibrillateur sous-cutané 1010 SQ-RX; programmation pour la procédure d'induction: Thérapies On, 1 zone (une zone de choc à 170 bpm), stimulation post-choc sur Off; gain sur 1X, vecteur primaire.
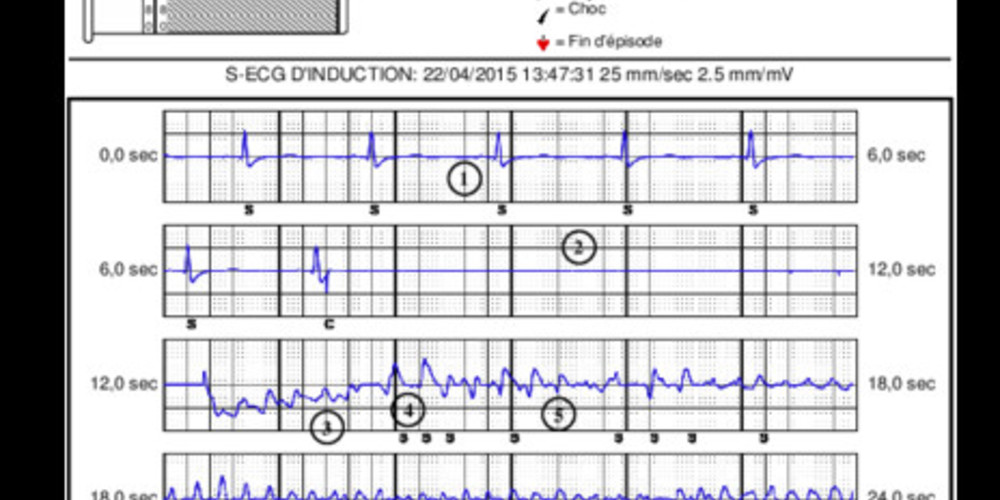
Tracé 8b
- rythme sinusal;
- burst 50 Hz délivré pendant 5 secondes environ;
- induction d'une FV (arythmie rapide, polymorphe, anarchique);
- premier cycle détecté classé S;
- plage de sous-détection devant l'atténuation de l'amplitude des signaux et la variation marquée de l'amplitude;
- détection intermittente de l'arythmie;
- premier cycle classé T, la moyenne des 4 intervalles précédents correspondant à la zone de tachycardie; le profil de sensibilité est modifié;
- sous-détection et cycles de nouveau classés S;
- détection correcte de l'arythmie avec cycles consécutifs classés T;
- le compteur 18/24 est rempli ainsi que le critère de persistance; début de la charge des condensateurs;
- poursuite de l'arythmie pendant la charge avec détection correcte;
- confirmation de l'arythmie en fin de charge;
- choc délivré (65 Joules) après 26 secondes d'arythmie;
- blanking post-choc;
- choc efficace et retour du rythme sinusal correctement détecté par le dispositif; bradycardie sans stimulation possible (stimulation post-choc programmée sur OFF).
Tracé 8c
Même patiente que tracé précédent; nouvelle induction en programmant le vecteur secondaire et la stimulation post-choc sur ON;
- burst 50 Hz délivré pendant 5 secondes environ;
- induction d'une FV (arythmie rapide, polymorphe, anarchique);
- premier cycle détecté classé S;
- les 4 premiers cycles détectés sont classés S;
- premier cycle classé T la moyenne des 4 intervalles certifiés précédents correspondant à une des 2 zones de tachycardie;
- détection correcte de l'arythmie avec cycles consécutifs classés T;
- le compteur 18/24 est rempli ainsi que le critère de persistance; début de la charge des condensateurs; sur les plateformes anciennes de défibrillateur, il était courant de voir un artéfact à la suite du début de la charge; cela explique pourquoi, les 2 premiers cycles suivant la charge n'adaptait pas le niveau de sensibilité;
- poursuite de l'arythmie pendant la charge;
- confirmation de l'arythmie en fin de charge;
- choc délivré (65 Joules);
- choc efficace; stimulation ventriculaire post-choc.





Les modes de détection et de classification des cycles cardiaques diffèrent complètement entre un défibrillateur endocavitaire et un défibrillateur sous-cutané. En effet, si un défibrillateur sous-cutané a pour objectif principal de détecter correctement et sans délai majeur un épisode d'arythmie ventriculaire pouvant compromettre la survie du patient, il n'y a pas de nécessité absolue de classer correctement chaque cycle en rythme sinusal ou lors d'un épisode d'arythmie. L'analyse des tracés retrouve fréquemment des cycles surdétectés, des cycles rapides sous-détectés ou incorrectement classés (extrasystoles ventriculaires classées . par exemple) ce qui pourrait s'avérer problématique pour un défibrillateur endocavitaire qui assure une fonction pacemaker nécessitant la détection parfaite de tous les cycles pour éviter une stimulation en période vulnérable. Les 2 priorités pour un défibrillateur sous-cutané sont donc d'éviter les thérapies inappropriées sur surdétection de l'onde T en rythme sinusal tout en conservant la capacité de détection des rythmes rapides ce qui justifie l'utilisation de profils différents de sensibilité en fonction de la fréquence cardiaque. Il existe de plus un certain nombre de différences fondamentales dans l'amplitude et la forme des signaux détectés par un défibrillateur sous-cutané par rapport aux signaux détectés par un défibrillateur endocavitaire. Ces différents éléments expliquent certaines différences de fonctionnement et de programmation:
- la pente et la fréquence des signaux enregistrés par des électrodes sous-cutanées sont plus faibles en rythme sinusal conduisant à l'enregistrement de complexes QRS plus "mous" moins différenciés de l'onde T ou de l'onde P; la valeur du filtre passe-haut est plus basse dans un défibrillateur sous-cutané que dans un défibrillateur endocavitaire (3 Hz vs. 14 – 20 Hz).
- les signaux enregistrés par les électrodes sous-cutanées sont plus larges que les signaux endocavitaires justifiant l'utilisation d'une période réfractaire post-détection plus longue pour éviter un double comptage de l'onde R; la durée de la période réfractaire varie en fonction de la fréquence des cycles détectés (plus courte en zone de choc) pour ne pas limiter la capacité de détecter des rythmes très rapides tout en minorant le risque de surdétection en rythme sinusal; la valeur de la période réfractaire n'est pas programmable (160 ms pour la zone de choc, 200 ms pour les cycles plus lents que la zone de choc).
- un défibrillateur sous-cutané fonctionne avec une valeur de sensibilité maximale plus élevée que celle d'un défibrillateur endocavitaire (0.08 mV versus 0.3 à 0.6 mV), l'amplitude des signaux intracardiaques enregistrés par des électrodes sous-cutanées étant globalement plus faible (amplitude des complexes QRS de 0.3 à 3.6 mV en rythme sinusal); le niveau de sensibilité maximale n'est pas programmable (0.08 mV, 80 µV) et reste le même quelle que soit la fréquence des signaux détectés et certifiés.
- le "signal-to-noise ratio" correspondant à la différence entre amplitude du signal à détecter (complexe QRS) et amplitude du "bruit" (onde P, onde T, myopotentiels, interférence électromagnétique) est plus faible; en effet, comme expliqué précédemment, l'amplitude des complexes QRS est moindre; de plus, les signaux extracardiaques sont d'amplitude plus importante, les électrodes sous cutanées étant beaucoup plus espacées que les électrodes bipolaires d'une sonde endocavitaire; un bon fonctionnement nécessite donc l'utilisation de filtres spécifiques permettant de rejeter les signaux à haute fréquence type 50 ou 60 Hz; une fois le signal détecté, la phase de certification permet de classer le cycle comme certifié ou comme bruit/surdétection; les signaux avec une fréquence trop élevée (myopotentiels, interférences, fracture de sonde) sont classés comme bruit et sont écartés du calcul de la fréquence cardiaque; les signaux passent ensuite à travers 4 étapes supplémentaires de certification pour diagnostiquer un double comptage de l'onde R ou une surdétection de l'onde T.
- les variations posturales de l'amplitude et de l'aspect des complexes QRS sont plus marquées que pour un défibrillateur endocavitaire impliquant l'utilisation d'un algorithme rectificatif pour atténuer ces variations.
- une sensibilité dynamique est utilisée pour réduire le risque de surdétection de l'onde T; une fois les signaux filtrés, le dispositif utilise un seuil de détection adaptatif en fonction de l'amplitude des 2 cycles certifiés précédents; le niveau de sensibilité augmente en parallèle à l'augmentation de la fréquence cardiaque pour optimiser les capacités de détection lors d'une tachycardie; différents profils de sensibilité (période réfractaire, niveau d'adaptation, retard d'adaptation) sont utilisés en fonction de la fréquence des signaux détectés, de la programmation (une seule zone ou 2 zones) et de la similitude de l'amplitude des 2 signaux certifiés précédents; aucun de ces paramètres n'est programmable; quand le rythme est lent, la priorité est de réduire au maximum le risque de surdétection de l'onde T, le profil de sensibilité est donc adapté (périodes réfractaires longues, niveau d'adaptation élevé, retard d'adaptation allongé d'autant plus que l'amplitude des 2 complexes certifiés précédents est différente); dans la zone de choc, l'objectif essentiel est d'optimiser la détection d'une éventuelle fibrillation ventriculaire avec des signaux rapides et d'amplitude variable ce qui implique l'utilisation d'une période réfractaire plus courte, d'un niveau d'adaptation relativement bas et d'un retard d'adaptation court.
- un défibrillateur sous-cutané n'assure pas de fonction pacemaker au long cours ce qui limite considérablement les contraintes en termes de nécessité de détection correcte cycle à cycle de l'intégralité des signaux (pas de risque de stimulation en période vulnérable); cela permet l'utilisation d'un système de comptage moyenné sur plusieurs cycles; pendant la phase de décision, le dispositif examine tous les cycles certifiés et calcule en continu une moyenne de fréquence ventriculaire sur 4 cycles RR certifiés; pour qu'un cycle soit considéré comme rapide il faut que la moyenne des 4 cycles soit rapide.
- en plus d'une zone de choc, le dispositif autorise une zone de choc conditionnel avec utilisation de 2 algorithmes d'analyse de la morphologie et 1 algorithme de mesure de la durée du QRS pour discriminer arythmies ventriculaires et arythmies supra-ventriculaires; l'existence d'électrodes de détection relativement distantes permet une analyse fiable de la morphologie des signaux avec toutefois une plus grande variabilité posturale; comme expliqué précédemment, la programmation d'une zone de choc conditionnel non seulement introduit une zone de discrimination mais modifie également le profil de détection.
L'intérêt principal d'un test d'induction en fin de procédure d'implantation est de pouvoir valider la qualité de la détection d'une FV avec le vecteur sélectionné. On retrouve schématiquement 3 profils différents:
Différents éléments influent sur la qualité de la détection d'un défibrillateur sous-cutané et peuvent expliquer ces différents tracés:
- comme expliqué précédemment, le système de comptage utilise une moyenne sur 4 cycles certifiés; il existe donc toujours une latence au diagnostic de quelques cycles en début d'arythmie; dans la plupart des cas, même quand la qualité de la détection est parfaite, on retrouve au début d'un épisode de FV un minimum de 3 à 4 cycles classés S.
- le niveau d'adaptation et le profil de sensibilité varient en fonction de l'amplitude moyennée des 2 signaux certifiés précédents; quand ces 2 signaux sont d'amplitude variable, le dispositif suspecte une surdétection (onde R de grande amplitude, onde T de plus faible amplitude4564) et applique le profil de sensibilité le moins élevé; lors d'un épisode de FV, arythmie par définition polymorphe et anarchique, il existe fréquemment une variabilité importante battements par battements de l'amplitude des signaux ce qui peut expliquer des plages plus ou moins importantes de sous-détection; cet élément peut expliquer pourquoi on peut retrouver un retard de détection au début de l'épisode (premier patient).
- différents profils de sensibilité sont appliqués en fonction de la fréquence cardiaque et de la programmation; quand la fréquence moyennée dépasse 168 battements par minute ou correspond à une zone de détection des arythmies, le dispositif devient plus sensible; cela explique pourquoi il est fréquent qu'après le premier cycle classé T, la qualité de la détection s'améliore et conduit à la succession de cycles T (premier patient); l'objectif du dispositif est donc de basculer lors d'un épisode d'arythmie d'un profil peu sensible (fait pour réduire les problèmes de surdétection) vers un profil plus sensible plus adapté à la détection d'une FV.
- la programmation influe directement sur la fréquence des arythmies devant être traitées (fréquence minimale pour détecter puis traiter une arythmie) mais, à la différence d'un défibrillateur endocavitaire, influe également directement sur la probabilité de détecter correctement les signaux; si l'on compare une programmation avec une seule zone de choc programmée à 200 battements par minute versus 2 zones avec une zone de choc conditionnel entre 200 et 230 battements par minute puis une zone de choc au-delà de 230 battements par minute: dans la zone conditionnelle, une discrimination des arythmies s'applique pour augmenter la spécificité; il faut toutefois intégrer que le dispositif est moins sensible en zone conditionnelle qu'en zone de choc (période réfractaire plus longue); pour une même valeur de fréquence (ici 200 battements par minute), le dispositif est donc moins sensible si une zone de choc conditionnel a été programmée; en revanche, si une seule zone de choc a été programmée au-delà de 230 battements par minute, rajouter une zone de choc conditionnel à partir de 200 battements par minute majore la capacité de détection des cycles rapides (défibrillateur devenant plus sensible entre 200 et 230 battements par minute); en résumé, plus la zone de choc est programmée pour des fréquences basses, plus l'appareil est sensible, le risque de sous-détection est donc moindre; à l'opposé, le risque de surdétection est plus élevé; la programmation avec 2 zones (zone conditionnelle entre 200 et 230 battements par minute puis une zone de choc au-delà de 230 battements par minute) parait un bon compromis entre capacité de détection correcte d'une FV et réduction des thérapies inappropriées; il parait étonnant dans ce cadre de tester le dispositif durant l'induction avec une seule zone de choc au-delà de 170 battements par minute puis de programmer 2 zones au long cours (zone conditionnelle entre 200 et 230 battements par minute puis une zone de choc au-delà de 230 battements par minute), le dispositif étant plus sensible durant l'induction et donc moins sujet à la sous-détection que pendant son fonctionnement au long cours; l'objectif de l'induction est à l'inverse de s'assurer d'une marge en termes de défibrillation mais également de qualité de la détection.
- modifier la position de la sonde a des effets incertains sur la qualité de la détection; les possibilités de reprogrammation en cas de sous-détection sont limitées à la limite des zones programmées et au vecteur de détection qui peut être modifié par l'opérateur; à partir de quel délai doit-on considérer que le retard de détection est trop important et justifie d'un test avec un second vecteur: 20 secondes, plus de 25 secondes? La réponse est délicate et ne s'appuie pas sur des éléments de littérature formels; après 20 secondes d'arythmie polymorphe, la perte de connaissance est certaine; pour le second patient, le délai avant le choc était tellement important qu'il a paru légitime à l'opérateur de changer le vecteur et de ré-induire; avec ce second vecteur, le délai avant le choc était alors bien moindre.