Surdétection de l'onde P et/ou de l'onde T
Homme de 25 ans avec syndrome de Brugada; implantation d'un défibrillateur sous-cutané Emblem A209; programmation: Thérapies On, 2 zones (une zone de choc conditionnel à 190 bpm, une zone de choc à 230 bpm), stimulation post-choc sur On; gain sur 2X, vecteur supplémentaire; consultation pour plusieurs chocs électriques au repos.
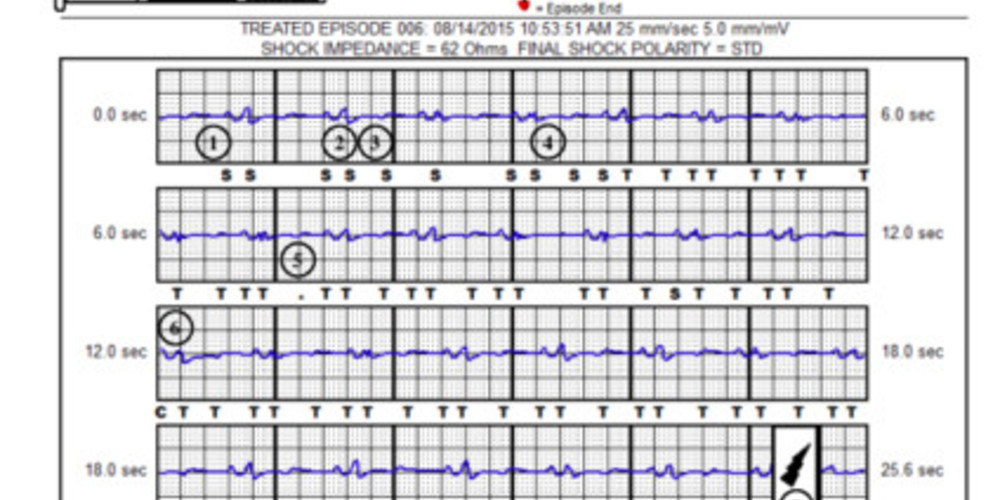
- surdétection de l'onde P;
- complexe QRS de petite amplitude (gain X 2);
- surdétection de l'onde T;
- détection pour un même cycle cardiaque de l'onde P, du complexe QRS et de l'onde T;
- cycle non certifié (diagnostic de surdétection par le dispositif);
- charge des condensateurs;
- choc électrique;
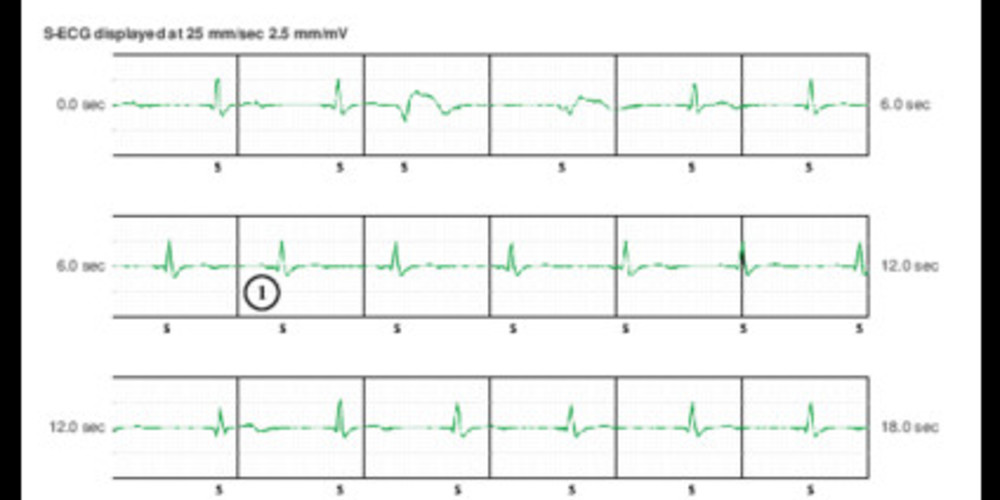
Enregistrement d'un tracé pour les 3 vecteurs avec un gain X 2; - vecteur supplémentaire; absence de surdétection ou de sous-détection en dépit d'un complexe QRS de petite amplitude et peu de différence entre amplitude de l'onde P et amplitude du complexe QRS;
- vecteur primaire; amplitude trop importante et complexe QRS "coupé" avec marqueur N;
- vecteur secondaire; amplitude trop importante et complexe QRS "coupé" avec marqueur N.
Homme de 53 ans avec myocardiopathie ischémique sévère; implantation d'un défibrillateur sous-cutané Emblem A209; programmation: Thérapies On, 2 zones (une zone de choc conditionnel à 200 bpm, une zone de choc à 220 bpm), stimulation post-choc sur On; gain sur 1X, vecteur secondaire; épisodes non traités enregistrés dans les mémoires.
- rythme sinusal;
- légère accélération de la fréquence avec complexes QRS élargis; probable RIVA;
- sudétection de la fin du complexe QRS/début de l'onde T;
- surdétection de l'onde T;
- alternance entre détection du complexe QRS (S) et du début de l'onde T (cycle non certifié, •); diagnostic correct de surdétection par le dispositif;
- absence de surdétection sur ce cycle;
- double surdétection sur ce cycle;
- persistance de la double surdétection;
- début de la charge des condensateurs;
- fin de la charge;
- réduction; complexe QRS identique au début du tracé;
- arrêt de la surdétection et fin de l'épisode.
Homme de 40 ans avec syndrome de Brugada; implantation d'un défibrillateur sous-cutané Emblem A209; programmation: Thérapies On, 2 zones (une zone de choc conditionnel à 200 bpm, une zone de choc à 230 bpm), stimulation post-choc sur Off; gain sur 1X, vecteur supplémentaire; hospitalisation à la suite de la survenue de plusieurs chocs électriques au cours d'un effort.

- tachycardie sinusale;
- surdétection de l'onde T;
- début de la charge des condensateurs;
- probable surdétection de myopotentiels; cycles non certifiés et classés N;
- fin de charge;
- le nombre de cycles consécutifs est ≥ au nombre de cycles requis;
- choc électrique;
- redétection;
- second choc électrique;
- troisième choc électrique;
- fin de l'épisode.
Homme de 32 ans avec dysplasie arythmogène du ventricule droit; implantation d'un défibrillateur sous-cutané 1010 SQ-RX; programmation: Thérapies On, 2 zones (une zone de choc conditionnel à 180 bpm, une zone de choc à 220 bpm), stimulation post-choc sur On; gain sur 1X, vecteur primaire; hospitalisation pour multiples chocs électriques puis syncope.

- enregistrement avec le vecteur primaire; complexe QRS de petite amplitude;
- tachycardie avec surdétection de l'onde T;
- alternance entre cycles classés T, S et •;
- charge des condensateurs; artéfact correspondant au début de la charge (N) classiquement observé sur les plateformes anciennes;
- premier choc électrique;
- second choc électrique;
- troisième choc électrique;
- quatrième choc électrique;
- induction d'une FV expliquant la syncope;
- cinquième choc électrique;
- réduction de l'arythmie.






Si la plupart des thérapies inappropriées observées chez des patients implantés d'un défibrillateur endocavitaire sont secondaires à un trouble du rythme supra-ventriculaire ou à un dysfonction de sonde, une surdétection de l'onde T représente la cause la plus fréquente de thérapies inappropriées pour les dispositifs sous-cutanés. La survenue de thérapies inappropriées était plus fréquente pour les premières plateformes de défibrillateur sous-cutané mais a sensiblement diminué sur les dispositifs plus récents. Cette baisse a été favorisée par la réalisation systématique d'une procédure de screening pré-implantatoire, la programmation en routine d'une zone conditionnelle et l'utilisation de nouveaux algorithmes durant les phases de détection et de certification.
Pour classer un cycle, 3 phases se succèdent: une phase de détection avec un filtrage du signal d'entrée, une phase de certification permettant de supprimer les signaux extracardiaques et une phase de décision. Ces 4 tracés permettent d'illustrer certaines spécificités du fonctionnement des défibrillateurs sous-cutanés en termes de détection et de certification:
- le dispositif utilise un seuil de détection adaptatif en fonction de l'amplitude des 2 cycles certifiés précédents. Pour le premier et le quatrième patient, la surdétection des ondes P et/ou des ondes T est favorisée par la faible amplitude des complexes QRS. Quand l'onde R est de petite amplitude, le dispositif atteint rapidement des niveaux élevés de sensibilité favorisant la surdétection de l'onde T particulièrement à l'effort (possible diminution de l’amplitude de l’onde R et légère augmentation de l’amplitude de l’onde T). Une onde R de petite amplitude est préférentiellement observée chez les patients avec dysplasie arythmogène du ventricule droit, syndrome du Brugada, sarcoïdose cardiaque ou myocardiopathie dilatée.
- le niveau de sensibilité augmente en parallèle à l'augmentation de la fréquence cardiaque pour optimiser les capacités de détection lors d'une tachycardie. En fonction de la fréquence, la durée des périodes réfractaires et l'adaptation du niveau de sensibilité dépendent de l'amplitude des signaux précédents et de la programmation. Pour une même borne basse de 200 bpm, programmer 2 zones avec une zone de choc conditionnel de 200 à 230 bpm rend le dispositif moins sensible et donc moins susceptible à la surdétection que programmer une seule zone de choc à 200 bpm.
- une fois le signal détecté, la phase de certification permet de classer le cycle comme certifié ou comme bruit/surdétection. Les signaux avec une fréquence trop élevée (myopotentiels, interférences, fracture de sonde) sont classés comme bruit et sont écartés du calcul de la fréquence cardiaque. Les signaux passent ensuite à travers 4 étapes supplémentaires de certification pour diagnostiquer un double comptage de l'onde R et/ou une surdétection de l'onde T.
Les différents algorithmes impliqués dans le diagnostic de surdétection de l'onde T, de l'onde P ou de l'onde R (double comptage) sont basés sur la mesure de l'amplitude minimale et maximale des complexes détectés, la mesure des délais entre les détections et de la largeur des signaux et sur la comparaison de la morphologie du signal détecté avec la morphologie du complexe précédent et la morphologie du complexe de référence.
- le premier algorithme compare la morphologie du signal détecté avec la morphologie de référence; le diagnostic de surdétection est suspecté devant la mise en évidence d'une alternance entre 2 signaux, un corrélé avec la référence, un non corrélé: répétition de séquences signal corrélé à signal non-corrélé à signal corrélé, suggérant la surdétection d'un signal cardiaque surnuméraire.
- le second algorithme recherche un double comptage des complexes QRS en recherchant un modèle répétitif d'alternance de morphologie sur des détections à couplage court et fixe.
- le troisième algorithme recherche une alternance entre la durée de 2 cycles (alternance entre 2 intervalles) et n'est donc pas basé sur une analyse de la morphologie du signal.
- le quatrième algorithme analyse la morphologie de 3 complexes détectés successifs et recherche la présence d'une séquence morphologie 1 (complexe QRS) - morphologie 2 (différente de la première; onde T) - morphologie 1 (complexe QRS); pour améliorer le rendement de l'algorithme, la largeur des complexes et les intervalles sont également intégrés dans l'analyse; le fonctionnement de cet algorithme ne dépend donc pas de la qualité de l'enregistrement de la morphologie de référence.
Quand un des algorithmes diagnostique une surdétection, le signal est non certifié avec un marqueur • sur le tracé sans spécification de quel algorithme a conduit au diagnostic.
Ces différents algorithmes peuvent être leurrés en cas de variabilité dans l'amplitude ou la morphologie des signaux, de surdétection intermittente ou de double surdétection. De plus, certains des algorithmes de diagnostic de surdétection n'ont été intégrés que sur les plus récentes plateformes et sont donc absents sur les dispositifs anciens. Une surdétection de l'onde T peut se compliquer de la survenue de multiples chocs inappropriés avec un risque d'induction d'une FV (tracé 18d), le choc pouvant être délivré en période vulnérable.
- le Smart Pass, disponible sur les dernières plateformes de défibrillateur a été conçu pour réduire l'occurrence de la surdétection de l'onde T. Il s'agit d'un filtre digital passe-haut, cet algorithme atténuant l'amplitude des signaux de basse fréquence. Les tracés utilisés pour la discrimination ne sont pas modifiés par cet algorithme. Les premiers résultats sont prometteurs. Quand le dispositif cherche automatiquement le vecteur optimal, le Smart Pass est activé si l'amplitude de tous les complexes QRS est ≥ 0.5 mV; quand une recherche manuelle du vecteur optimal est privilégiée, le Smart Pass est activé si sur une durée de 16 secondes, au minimum 5 complexes QRS consécutifs ont une amplitude ≥ 0.5 mV. Il est possible de déprogrammer le Smart Pass à partir de l'écran Smart Settings. Le dispositif désactive également automatiquement le Smart Pass si il suspecte une sous-détection dans les conditions suivantes: signaux de petite amplitude (≤ 0.25 mV) et pauses ventriculaires (≥ 1.4 secondes) ou épisode d'asystolie de plus de 10 secondes. L'avantage de cet algorithme est donc de réduire la surdétection de l'onde T au prix d'un risque accru de sous-détection d'un épisode de FV.