Ecoute croisée ventriculaire par le canal atrial
Homme de 74 ans, implanté d'un stimulateur cardiaque double chambre Ensura DR dans le cadre d'un bloc auriculo-ventriculaire complet post-chirurgie d'une valve aortique; sonde auriculaire positionnée au niveau de l'auricule droit, sonde ventriculaire positionnée au niveau du septum haut; patient asymptomatique, visite de contrôle 3 mois après l'implantation.
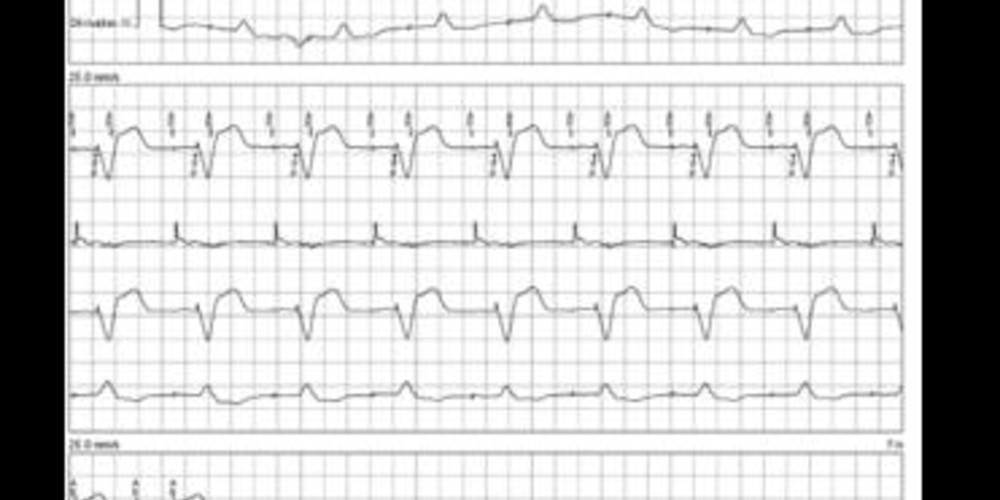
Tracé 17a:
Tracé enregistré à l'arrivée; programmation en mode DDDR; la première ligne correspond à la dérivation DI sur laquelle se superposent les marqueurs, la seconde ligne correspond à l'EGM atrial, la troisième ligne à DII et la dernière à DIII;
- séquences AP-VP-AR avec intervalles VP-AR fixes; la stimulation atriale semble efficace; l'EGM atrial montre la dépolarisation atriale suivant les différents AP confirmant une capture atriale effective; capture ventriculaire efficace; derrière chaque VP, l'EGM atrial montre un signal de petite taille correspondant probablement à l'écoute croisée du ventricule par le canal atrial;
Tracé 17b:
Changement de programmation avec prolongation du blanking atrial post-ventriculaire;
- même tracé et même programmation que le précédent;
- changement de programmation avec allongement du blanking (programmation blanking partiel);
- le signal atrial détecté derrière chaque stimulation ventriculaire est identique mais est à présent détecté dans le blanking atrial post-ventriculaire (intervalles VP-Ab fixes);
Tracé 17c:
Modification de la programmation (blanking partiel vers partiel plus);
- même tracé et même programmation que le précédent;
- changement de programmation (blanking partiel plus);
- disparation de l'écoute croisée.





Le blanking atrial post ventriculaire constitue la première partie de la période réfractaire atriale post-ventriculaire. Traditionnellement, aucune détection n'était possible dans une fenêtre identifiée comme un blanking qui constituait une période réfractaire absolue. Sur les nouvelles plateformes de stimulateurs, cette différentiation entre blanking (absence de détection et absence de visualisation du signal sur la chaine de marqueurs) et périodes réfractaires (détection possible avec visualisation sur la chaine de marqueurs) est moins nette. En effet, en fonction de la programmation, un évènement atrial détecté pendant le "blanking" atrial post ventriculaire peut être visualisé sur la chaine de marqueurs et interférer avec le fonctionnement de différents algorithmes. Il existe 3 options de programmation:
Un signal détecté dans le BAPV (classé Ab) comme un signal détecté dans la PRAPV (classé AR) ne déclenche pas de délai AV mais est comptabilisé pour le diagnostic des arythmies atriales.
Chez ce patient, le diagnostic d'écoute croisée est évident. Le signal atrial surnuméraire détecté est de petite taille et très précoce par rapport à la stimulation ventriculaire. Pour éviter l'écoute croisée, 4 solutions sont envisageables: